在与病原微生物的长期协同进化中,植物构建起多层次防御体系,化学防御是其中抵御入侵的关键防线。植保素是植物感知病原后快速合成的小分子抗微生物次生代谢物,可直接抑制、杀灭病原体,是植物化学防御的核心物质。自植保素概念提出 80 余年来,多数植保素的生物合成途径与调控机制仍未破解,严重限制其在作物抗病中的应用转化。
德布尼醇(debneyol)是烟草、辣椒等茄科植物特有的倍半萜类植保素,与经典植保素辣椒醇(capsidiol)共享 5-表-马兜铃烯(5-EA)前体,且具备更强的广谱抗真菌活性。自 1979 年被发现以来,其完整生物合成通路近半世纪始终未被解析,成为植物防御领域的长期难题。
2026年5月8日,william威廉中文官网雷晓光团队与清华大学生命科学学院刘玉乐团队合作研究在《Cell》期刊在线发表题为“植保素介导植物化学防御的遗传基础(Genetic basis of phytoalexin-mediated chemical defense in plants)”的研究论文。该研究完整解析并成功重构了植保素德布尼醇(debneyol)的生物合成通路,同时揭示了miR1919-MCD1模块在该通路中的核心调控作用机制,并进一步证明MCD1可通过组织多酶复合物实现代谢流的精准导向至debneyol合成,显著增强植物对真菌、病毒和细菌的广谱抗病能力(图1)。上述成果不仅阐明了植保素debneyol介导植物化学防御的遗传学基础,也为通过基因工程创制广谱抗病作物以及利用合成生物学手段规模化生产广谱抗病化合物debneyol奠定了坚实基础。
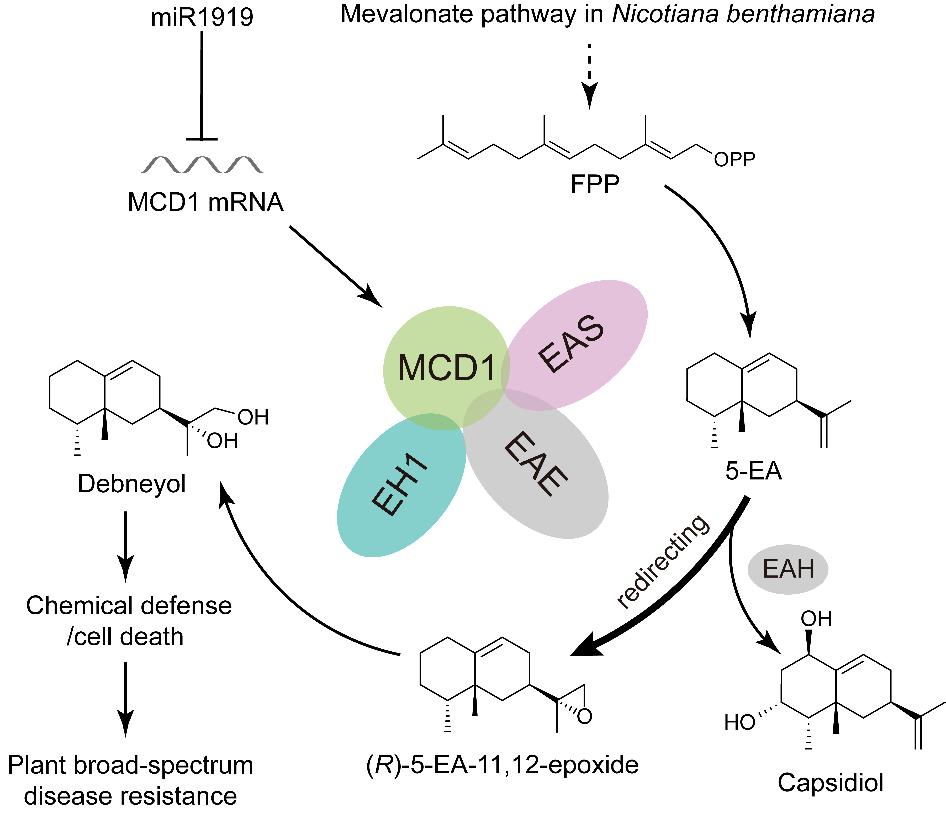
图1:广谱抗病植保素德布尼醇(debneyol)生物合成与调控
在本研究中,团队鉴定到一个茄科植物特有的miR1919及其靶基因MCD1。沉默miR1919或过表达MCD1会触发强烈的植物细胞死亡,并伴随debneyol的积累。在此基础上,团队鉴定到MCD1可与5-EA合成酶(EAS)互作,EAS负责催化法尼基焦磷酸(FPP)环化生成5-EA。进一步发现,MCD1诱导的细胞死亡依赖EAS活性,且MCD1显著改变5-EA下游代谢产物的分布。农杆菌侵染时另一类倍半萜天然产物capsidiol及其乙酰化衍生物大量积累,debneyol不可检测;而MCD1过表达时,debneyol大量积累。这表明MCD1将代谢流从capsidiol分支重定向至debneyol分支。
为阐明其分子机制,研究团队整合多组学与生化分析,解析了debneyol的完整生物合成路径:以FPP为前体,依次经EAS、5-EA环氧化酶(EAE)和环氧化物水解酶1(EH1)三步催化生成终产物debneyol。具体而言, EAS催化FPP生成5-EA,EAE将其转化为(R)-5-EA-11,12-epoxide(5-EA-11,12-环氧化物),随后EH1进一步水解生成debneyol(图1)。该研究首次完整解析并在酵母中重构了debneyol从FPP到终产物的三步生物合成通路,解决了自1979年其被发现以来长期未解的生化机制问题。
最令人兴奋的发现来自MCD1的作用机制。MCD1不仅转录上调EAS、EAE、EH1等基因的表达,更关键的是,其还是一个代谢组织者(metabolic organizer),通过组装EAS-EAE-EH1多酶复合物,增强EAE的催化活性并诱导底物通道效应(substrate channeling),将代谢流从capsidiol分支“重定向”至debneyol分支,从而高效地引导前体5-EA进入广谱抗病化合物debneyol的合成(图1)。这一发现拓展了人们对代谢调控的认知: 除了经典的转录调控和翻译后修饰,植物还可以通过代谢组织者的空间组织和活性调节,实现对代谢分支的精准控制。
团队进一步发现,debneyol的积累与细胞死亡程度及抗病性呈正相关。在MCD1过表达的植物中,debneyol大量合成,植株表现出对病毒(烟草坏死病毒)、真菌(灰霉菌、链格孢菌)和细菌(假单胞杆菌)等多种病原体的广谱抗性。重要的是,利用病原诱导型启动子TBF1及其上游开放阅读框(uORFs)驱动MCD1在本生烟草中表达,可在不影响植物正常生长的情况下,实现植物对跨界病原的广谱抗性。
该研究完整阐明了植保素debneyol的生物合成通路(由EAS、EAE、EH1三步酶促反应构成)及其核心调控机制(通过miR1919-MCD1模块),揭示了植物化学防御中一个此前未知的遗传与分子通路,尤其是MCD1作为“代谢组织者”组装EAS-EAE-EH1多酶复合物,增强EAE的催化活性并诱导底物通道效应,实现代谢流由capsidiol分支向debneyol分支的重定向,从而高效合成广谱抗病化合物debneyol。这些发现为培育广谱抗病作物提供了新的基因资源和设计策略,并为通过基因工程创制广谱抗病作物及利用合成生物学规模化生产debneyol奠定了坚实基础。
清华大学生命科学学院刘玉乐教授、北京大学雷晓光教授及其团队副研究员高磊博士(现武汉大学药学院教授)为本论文的共同通讯作者;王占理(清华大学博士生)、韩璐(清华大学2022届博士毕业生)以及高磊教授为论文的共同第一作者。 本研究得到了国家自然科学基金、国家重点研发计划、北大-清华生命科学联合中心、新基石科学基金会、北京分子科学国家研究中心等项目或机构的支持。
论文链接:https://doi.org/10.1016/j.cell.2026.04.021
排版:高杨
审核:牛林,刘志博